强生(JNJ)旗下杨森制药近日在美国视网膜专家学会(ASRS)2020年虚拟年会上公布了正在进行的I/II期试验MGT009(NCT03252847)的6个月数据。该试验正在评估在研基因疗法AAV-RPGR(腺相关病毒视网膜色素变性GTPase调节剂,通过视网膜下注射给药)治疗遗传性视网膜疾病X连锁视网膜色素变性(XLRP)。中期数据显示,低剂量和中等剂量的AAV-RPGR的耐受性良好,并表明视力有改善。
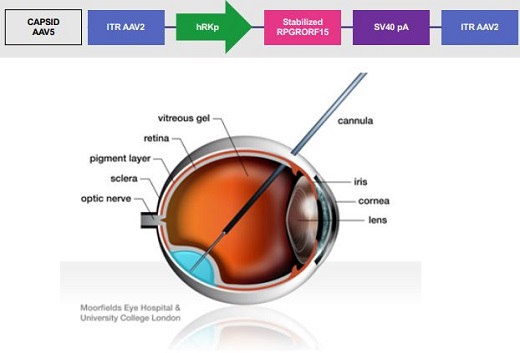
AAV-RPGR是一种在研基因疗法,用于治疗由眼睛特异性RPGR基因(RPGR 0RF15)中的突变导致XLRP的患者。AAV-RPGR旨在将RPGR基因的功能拷贝递送至视网膜下空间,改善和维持视觉功能。AAV-RPGR由杨森与MeiraGTx Holdings公司联合开发,用于治疗RPGR ORF15突变的XLRP患者。此次公布的数据也是来自双方合作的首次数据发布。
根据这项研究的数据,欧洲药品管理局(EMA)授予了AAV-RPGR优先药物(PRIME)和先进医疗产品(ATMP)资格,这项资格认定将增加监管互动并优化开发计划。美国食品和药物管理局(FDA)还授予了AAV-RPGR快速通道资格(FTD)。此外,EMA和FDA还授予了AAV-RPGR孤儿药资格(ODD)。
在XLRP患者中,眼睛中负责将光转换为信号并发送到大脑的光感受器功能低下,导致视网膜退化,成年后失明。AAV-RPGR是一款在研基因疗法,用于治疗由RPGR基因突变引起的常见和严重的XLRP,通过减缓视网膜退化,保护和改善视力。针对该疾病,目前还没有批准的治疗方法。
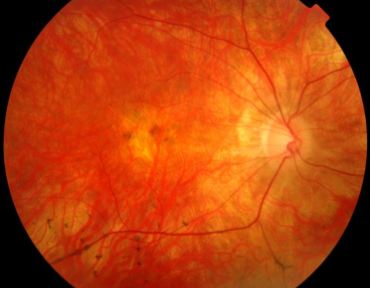
XLRP(图片来源:oxfordbrc.nihr.ac.uk)
这项正在进行的I/II期临床试验分为三个阶段:剂量递增、剂量确认和剂量扩展。在剂量递增阶段(n=10),成人患者接受低、中、高剂量AAV-RPGR治疗。AAV-RPGR通过视网膜下注射给药,靶向在基线时受影响较大的一只眼睛的中央视网膜,患者的另一只眼作为非治疗对照。研究中,允许多次视网膜切开术来覆盖可挽救视网膜的较大可能区域。
使用Octopus 900全视野静态视野检查和MAIA眼底引导显微视野检查进行视野检查(Perimetry),并在基线、3个月、6个月、9个月和12个月进行,以评估基线视网膜功能和随时间的变化。患者需要有黄斑部视网膜结构相对保留的证据,并能够进行与年龄相适应的临床评估。视野检查(Perimetry)是评价视网膜功能的一种敏感的标准方法,可重复性地确定视网膜在横截面和纵向上的敏感性,从而准确地确定疾病随时间的进展。该试验的主要终点是安全性,次要终点是在治疗后预先指定的时间点评估视觉功能的变化。
在剂量递增阶段,治疗6个月时,低剂量组(n=3)和中剂量组(n=4)显示治疗后视网膜敏感性较基线有改善。重要的是,当用2种视野检查法(静态视野检查法和显微视野检查法)和三种分析测量法(平均视网膜灵敏度、中心30°视野希尔体积测量法[V30]和逐点比较法)进行评估时,这些改善是明显的。
I/II期试验参与者的这些中期结果表明,研究结果具有重要意义:(1)在中剂量组,治疗眼和未治疗眼的平均视网膜敏感性存在显著差异:1.02分贝(dB);(90%CI:0.75,1.31)。(2)在低剂量组(1.10 dB-sr(steradian,球面度)/年;(90%CI:0.10,2.10)和中等剂量组(1.26 dB sr/年)(90%CI:0.65,1.86),治疗眼和未治疗眼的中心视野进展率(V30)存在显著差异。(3)在3个月时进行的治疗后评估中观察到疗效信号,并且在6个月时持续改善或改善增加。
迄今为止获得的安全数据具有可预期和可管理的眼部和系统安全性。常见的不良事件与外科手术有关,短暂且无需干预即可解决。在高剂量组(n=3)中,三分之二的成人患者有明显的炎症反应,视觉功能的测量没有改善。
杨森研发公司心血管和新陈代谢全球治疗领域负责人James List博士表示:“这些发现证明了我们在研AAV-RPGR基因疗法的潜力,不仅可以保护XLRP患者的视力,还可以改善XLRP患者的视力。我们对迄今所见的数据感到鼓舞,并期待着分享未来数据以及推进我们的临床开发项目。”
2019年1月,杨森与临床阶段基因治疗公司MeiraGTx Holdings plc签订了全球合作和许可协议,以开发、制造和商业化其临床阶段遗传性视网膜疾病产品组合。AAV-RPGR基因治疗是在这个合作和许可协议下开发的。除了形成研究合作,探索其他遗传性视网膜疾病的新靶点外,杨森还与MeiraGTx合作,建立病毒载体设计、优化和制造的核心能力。
除了AAV-RGRP,双方也正在开发用于治疗全色盲的2款基因疗法AAV-CNGB3和AAV-CNGA3,这2种基因疗法通过视网膜下注射递送至视网膜内大多数锥体细胞所在的眼睛区域,以恢复锥体细胞的功能。AAV-CNGB3在美国已被授予孤儿药资格(ODD)、罕见儿科疾病资格、快速通道资格(FTD),在欧盟已被授予孤儿药资格(ODD)和优先药物资格(PRIME)。
原文出处:Interim Six-Month Data of RPGR Gene Therapy Shows Significant Vision Improvement in Patients Living with X-Linked Retinitis Pigmentosa
声明:本文版权归原作者所有,转载文章仅为传播更多信息,如作者信息标记有误,或侵犯您的版权,请联系我们,我们将在及时修改或删除内容,联系邮箱:marketing@360worldcare.com

