在阿尔茨海默症(AD)早期,tau蛋白在大脑突触中积聚,破坏信号在神经元之间的传递。tau蛋白的积聚被认为与阿尔茨海默病患者认知能力下降有关,而且tau越多,认知退化的速度就越快。
许多研究都试图通过清除或降低有毒的tau蛋白积聚来提高阿尔茨海默症患者的认知能力,在5月26日发表于Science Translational Medicine上的一项新研究中,哥伦比亚大学欧文医学中心的研究人员发现了一种更为精确地清除有毒tau蛋白的方法。
在先前的研究中,研究人员发现tau蛋白的水平可以通过提高蛋白酶体的活性来降低,但是在多种神经退行性疾病研究中已观察到负责降解tau蛋白的26S蛋白酶体的活性被损伤。
“我们不想将整个细胞中的蛋白降解都增加,过多的降解可能会产生一些不良影响。” 论文通讯作者Natura Myeku博士说。所以研究人员需要找到tau蛋白的积聚处并进行精准打击,尤其是那些毒性强的tau蛋白。
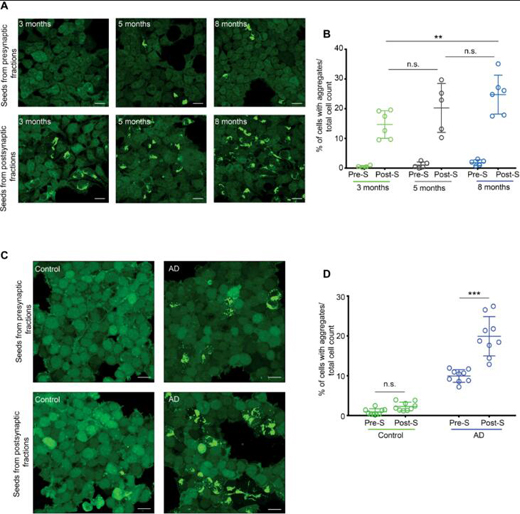
Tau蛋白病的一个基本特征是具有传播力(seeding activity)的tau蛋白会优先经突触在大脑中转运。在这项新研究中,研究人员发现,这种tau蛋白主要聚集在突触后区室,而且检测到了蛋白酶体的受损加剧了区室内tau蛋白介导的毒性。

突触后的tau蛋白表现出高传播活性(来源:Science Translational Medicine)
研究人员试着通过提高这一侧蛋白酶体的活性实现tau蛋白的降解,不影响大脑其它部位的蛋白酶体。
他们利用垂体腺苷酸环化酶激活肽(Pituitary Adenylate Cyclase Activating Polypeptide, PACAP)刺激其1型受体(PAC1R),PAC1R是一种G蛋白偶联受体(GPCR),且大部分PAC1R与“种子”tau蛋白位于突触同侧。
结果表明,PACAP与PAC1R结合后,26S蛋白酶体活性增强,而且有毒tau蛋白的水平发生降低,处在tau蛋白积聚早期的小鼠的认知能力也被改善,重要的是,这种肽对突触的另一侧几乎没有影响。
PACAP刺激后有毒tau蛋白(黄色)的数量减少,左右图分别为未接受处理和处理后的神经元(来源:Science Translational Medicine)
不过,PACAP在体内会迅速降解,不是一种理想的治疗方法,因此,研究人员目前正在测试另一种药物普芦卡必利,普芦卡必利是一种治疗胃肠道疾病的5-HT4R激动剂,5-HT4 受体与PAC1R具有相似作用。
总的来说,这项研究揭示了激活PAC1R可以防止有毒tau蛋白的积累,并为阿尔茨海默症和其它tau蛋白相关的疾病提供了一种有希望的治疗方法。
声明:本文版权归原作者所有,转载文章仅为传播更多信息,如作者信息标记有误,或侵犯您的版权,请联系我们,我们将在及时修改或删除内容,联系邮箱:marketing@360worldcare.com

