Zynlonta治疗恶性淋巴瘤疗效显著 在中国已获批临床试验
瑞士生物技术公司ADC Therapeutics SA近日在第16届国际恶性淋巴瘤年会(ICML)上公布了CD19靶向性抗体偶联药物(ADC)Zynlonta(loncastuximab tesirine-lpyl)2项临床试验的新数据。
来自LOTIS-2试验的结果证明了Zynlonta的持久反应,在过度预治疗(heavily-preteated,指先前接受过多种疗法)的复发或难治性弥漫性大B细胞淋巴瘤(DLBCL)患者中的中位缓解持续时间(DOR)达到了13.4个月。来自LOTIS-3试验的结果,突出了Zynlonta联合伊布替尼(ibrutinib,BTK抑制剂)在复发或难治性DLBCL和套细胞淋巴瘤(MCL)患者中的潜力。
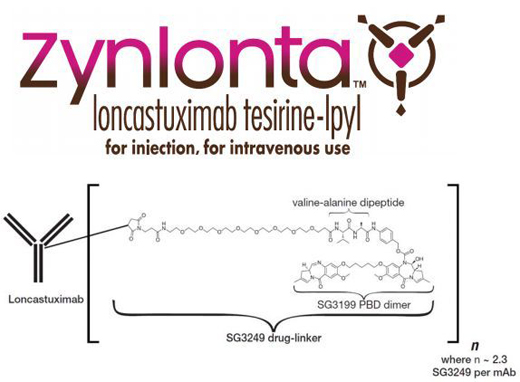
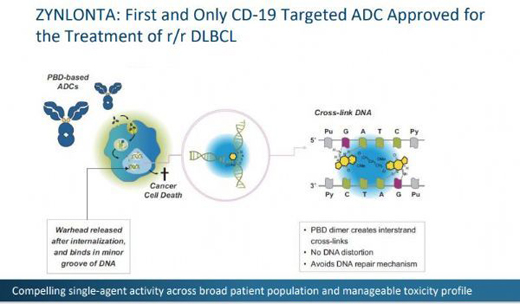
Zynlonta是一种靶向CD19的抗体偶联药物(ADC),该药活性药物成分为loncastuximab tesirine,由一种人源化抗人CD19单克隆抗体通过连接子与吡咯并苯并二氮杂卓(pyrrolobenzodiazepine,PBD)二聚体细胞毒素偶联而成。一旦与表达CD19的细胞结合,loncastuximab tesirine就会被细胞内化,随后释放出细胞毒素,该毒素能不可逆地与DNA结合,从而产生阻止DNA链分离的强力链间交联,从而破坏复制等必要的DNA代谢过程,导致细胞死亡。CD19是一个经验证的治疗B细胞恶性肿瘤的热门靶点。
loncastuximab tesirine分子结构
2021年4月,Zynlonta获得美国FDA加速批准,用于治疗已接受过2种或多种系统疗法的复发或难治性(r/r)大B细胞淋巴瘤(LBCL)成人患者,包括弥漫性大B细胞淋巴瘤(DLBCL)、起源于低级别淋巴瘤和高级别细胞淋巴瘤的DLBCL。
在中国,Zynlonta正由ADC Therapeutics与瓴路药业(Overland Pharmaceuticals)成立的合资公司Overland ADCT BioPharma开发。根据中国国家药品监督管理局(NMPA)药品审评中心(CDE)检索结果,Zynlonta在中国已获得一项临床试验模式许可(受理号:JXSL2000231)。
值得一提的是,Zynlonta是一个也为少有一个CD19靶向ADC,作为单一制剂治疗r/r DLBCL成人患者。该药的批准上市,将解决广泛的三线和多线(3L+)r/r DLBCL患者群体中的未满足医疗需求,包括未另行指定的DLBCL、源于低级别淋巴瘤和高级别B细胞淋巴瘤的DLBCL患者。来自关键LOTIS-2试验的数据显示,在过度预治疗(heavily-preteated,指先前接受过多种疗法)r/r DLBCL患者中,Zynlonta单药治疗的总缓解率(ORR)达到了48.3%、完全缓解率(CR)为24.1%,并且缓解持久(详见:Zynlonta FDA Approval Presentation)。
Zynlonta作用机制
LOTIS-2试验随访分析数据:
LOTIS-2是一项单臂、开放标签临床试验(n=145),在先前接受过至少2种系统疗法治疗失败的复发或难治性DLBCL患者中开展,评估了Zynlonta单药治疗的疗效和安全性。共145例患者入组研究,这些患者先前接受的系统疗法中位数为3种。截至2021年3月1日数据截止日期,所有患者均已完成治疗。
此次公布的结果显示,Zynlonta单药治疗显示出持续的抗肿瘤活性和可接受的安全性。关键数据包括:总缓解率(ORR)为48.3%(70/145例)、完全缓解率(CRR)为24.8%(36/145例)。在病情缓解的70例患者中,中位缓解持续时间(DOR)为13.4个月。病情完全缓解的36例患者中,中位DOR尚未达到。中位总生存期(OS)为9.5个月。该研究中,没有发现新的安全性问题,与<65岁的患者相比,在≥65岁的患者中没有观察到毒性增加。常见的≥3级治疗期间不良事件(TEAE)为中性粒细胞减少(26.2%)、血小板减少(17.9%)、γ-谷氨酰转移酶升高(17.2%)和贫血(10.3%)。
LOTIS-3试验随访分析数据:
LOTIS-3是一项1/2期、两部分、开放标签、单臂临床试验,正在评估Zynlonta联合伊布替尼(ibrutinib,BTK抑制剂)治疗复发或难治性DLBCL或MCL的疗效。更新的1期结果截至2021年3月1日,30例DLBCL患者(24例为非生发中心B细胞[non-GCB]DLBCL,6例为生发中心B细胞[GCB]DLBCL)和7例MCL患者被纳入研究。
关键数据包括:在所有患者中的ORR为62.2%、CRR为35.1%。在non-GCB-DLBCL患者中,ORR为66.7%;在GCB-DLBCL患者中,ORR为16.7%。在MCL患者中,ORR为85.7%。Zynlonta与伊布替尼联合用药具有可控的毒性,发生在≥5%患者中的常见≥3级TEAE为贫血(10.8%)、中性粒细胞减少(10.8%)、血小板减少(5.4%)、疲劳(5.4%)。截至第2周期的药代动力学特征显示持续暴露和适度积累。
原文出处:ADC Therapeutics Presents Updated ZYNLONTA (loncastuximab tesirine-lpyl) Clinical Data at 16th Annual International Conference on Malignant Lymphoma
声明:本文版权归原作者所有,转载文章仅为传播更多信息,如作者信息标记有误,或侵犯您的版权,请联系我们,我们将在及时修改或删除内容,联系邮箱:marketing@360worldcare.com