复发难治经典霍奇金淋巴瘤,有哪些值得关注的治疗方案?
第17届国际恶性淋巴瘤会议(ICML)于近期召开,会上公布多项复发难治(R/R)经典霍奇金淋巴瘤(cHL)相关研究进展,对部分药物在R/R cHL中的疗效和安全性进行了探索。小编现将研究主要内容整理如下,供广大读者参考。
摘要74:纳武利尤单抗治疗R/R cHL:II期CheckMate 205研究5年生存结果
研究背景
以单克隆抗体纳武利尤单抗为代表的PD-1免疫检查点抑制剂在R/R cHL中展现出较好的活性。II期CheckMate 205研究(NCT02181738)结果显示,中位随访18个月时,纳武利尤单抗治疗R/R cHL的客观缓解率(ORR)为69%,中位缓解持续时间(DOR)为17个月,中位无进展生存期(PFS)为15个月。但目前尚不清楚PD-1抑制剂治疗R/R cHL的治疗持续时间和长期生存获益情况。现公布CheckMate205研究中位随访58个月时的新研究结果。
研究方法
CheckMate 205研究纳入自体造血干细胞移植后疾病进展或复发的R/RcHL患者,根据维布妥昔单抗治疗情况分为A(未接受过维布妥昔单抗治疗)、B(移植前未接受过维布妥昔单抗治疗且移植后接受过维布妥昔单抗治疗)、C(移植前接受过维布妥昔单抗治疗)三个队列。
患者每2周接受纳武利尤单抗3mg/kg治疗,直至疾病进展或出现不可耐受的不良反应。队列C患者在完全缓解(CR)达到1年后停用纳武利尤单抗,如果在2年内疾病复发可恢复纳武利尤单抗的治疗。研究主要终点为独立评审委员会(IRC)评估的ORR,次要终点包括CR、DOR、PFS、总生存期(OS)、安全性。
研究结果
研究共纳入243例患者(队列A、B、C分别有63、80、100例患者),中位接受纳武利尤单抗治疗14个月。ORR为71%(95%CI:65%-77%),CR率为21%,中位PFS为15个月(95%CI:11-19),中位DOR为18个月(95%CI:15-26)。相比于部分缓解(PR)患者,CR患者中位PFS(37个月 vs 15个月)和中位DOR(30个月 vs 13个月)均更长。2年OS率为87%(95%CI:82%-91%),2年PFS率为37%(95%CI:30%-44%);5年OS率为71%(65%-77%),5年PFS率为18%(95%CI:12%-25%)。CR患者的OS同样得到改善,未能达到疾病稳定为OS的不良预后因素。
队列C中12例患者在CR达到1年后停用纳武利尤单抗。这部分患者中位停药48个月(范围:36-55),6例患者仍处在疾病缓解状态,3例患者在疾病进展后重新开始纳武利尤单抗治疗(2例患者重新达到CR,1例患者达到PR)。
研究中未观察到新的毒性事件。常见的治疗相关不良事件(TRAE)为疲劳(25%)、腹泻(17%)、皮疹(12%),大部分TRAE为1-2级。68例(28%)患者出现3-4级TRAE,26例(11%)患者因TRAE停药,未出现治疗相关的死亡事件。
研究结论
CheckMate 205研究5年分析结果显示,纳武利尤单抗治疗R/R cHL可获得较好的OS,安全性与既往研究报告结果相似,证实了该药在移植后疾病进展或复发的R/R cHL患者中的有效性和安全性。R/R cHL患者接受纳武利尤单抗治疗达到CR状态1年后可以尝试停药。
摘要75:Camidanlumab tesirine单药治疗R/R cHL的疗效和安全性:一项开放标签、多中心II期研究结果
研究背景
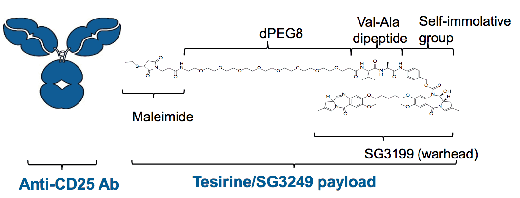
Camidanlumab tesirine(Cami)是一种靶向CD25的单克隆抗体与吡咯并苯二氮卓二聚体(PBD)偶联生成的抗体药物偶联物。Cami在淋巴瘤,尤其是R/R cHL的相关I期研究中展现出令人鼓舞的抗肿瘤活性和可控的安全性。在此公布Cami单药治疗R/RcHL的II期研究初步结果。
研究方法
研究纳入先前接受≥3线治疗(包括维布妥昔单抗和PD-1抑制剂)或先前接受≥2线治疗且不适合接受移植的R/R cHL患者,接受Cami单药治疗(每个21天治疗周期的第1天接受Cami 45μg/kgIV,持续2周期,随后每周期接受Cami30μg/kg IV)。研究的主要终点为ORR,次要终点包括DOR和PFS。
研究结果
截至2020年12月4日,研究共纳入82例R/R cHL患者,中位接受过7线(范围:3-19)治疗。患者平均接受了4个周期的Cami治疗。47例停止Cami治疗的患者中,5例(10.6%)患者随后接受了移植。
52例患者疗效可评估,ORR为82.7%(43/52),CR率为38.5%(20/52)。中位随访时间9.2个月(范围:2.0-14.3)时,中位DOR未达到,中位PFS为9.2个月(95%CI:5.0-NR)。
82例患者中发生率≥25%的治疗期间不良事件(TEAE)包括疲劳(34例,41.5%)、恶心(23例,28.0%)、丘疹(23例,28.0%)、发热(21例,25.6%)。
声明:本文版权归原作者所有,转载文章仅为传播更多信息,如作者信息标记有误,或侵犯您的版权,请联系我们,我们将在及时修改或删除内容,联系邮箱:marketing@360worldcare.com