恶性胸膜间皮瘤 Opdivo+Yervoy免疫组合在中国台湾获批
小野制药(Ono Pharmaceutical)近日宣布,中国台湾药品监管部门已批准抗PD-1疗法Opdivo(欧狄沃,通用名:nivolumab,纳武单抗)联合抗CTLA-4疗法Yervoy(ipilimumab,易普利姆玛),一线治疗恶性胸膜间皮瘤(MPM)成人患者。
Opdivo+Yervoy是2种免疫检查点抑制剂的独特组合,具有潜在的协同作用机制,针对2个不同的检查点(PD-1和CTLA-4)来帮助摧毁肿瘤细胞。
在美国和欧盟,Opdivo+Yervoy方案分别于2020年10月、2021年6月获得批准,一线治疗不可切除性MPM成人患者。值得一提的是,Opdivo+Yervoy方案是过去15年来一个被证实可改善MPM患者生存的新疗法。
此次批准基于关键3期CheckMate-743试验的结果,这是一线治疗MPM的一个阳性3期免疫治疗试验。结果显示,在所有随机化患者中,与化疗(培美曲塞和顺铂或卡铂)相比,Opdivo+Yervoy双重免疫疗法(OY组合)显示出持久的生存益处,达到了延长总生存期(OS)的主要终点。
CheckMate-743是一项开放标签、多中心、随机III期临床试验,共入组了605例先前未经治疗的、无法切除的MPM患者,评估了Opdivo+Yervoy双重免疫疗法用于一线治疗的疗效和安全性,并与化疗(培美曲塞+顺铂或卡铂)进行比较。研究中,患者随机分配,接受Opdivo+Yervoy(n=303)、化疗(n=302)治疗。Opdivo+Yervoy治疗组,Opdivo每两周一次给药3mg/kg,Yervoy每六周一次给药1mg/kg,持续24个月或直到疾病进展或出现不可接受的毒性。化疗组,接受顺铂75mg/m2或卡铂AUC 5联合培美曲赛500mg/m2,21天为一个周期,共6个周期,或直到疾病进展或出现不可接受的毒性。研究主要终点是所有随机患者的总生存期(OS)。
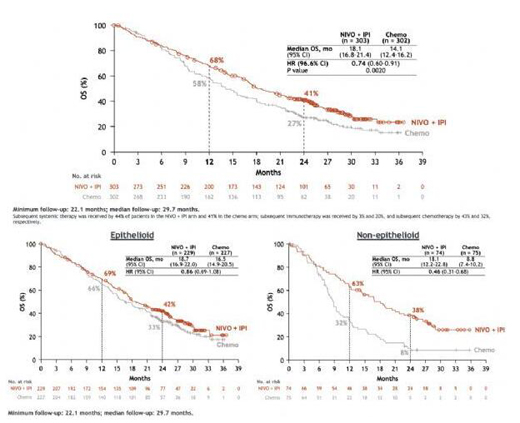
结果显示,研究达到主要终点:与化疗组相比,Opdivo+Yervoy组OS有显著改善(中位OS:18.1个月 vs 14.1个月)、死亡风险降低26%(HR=0.74;95%CI:0.61-0.89;p=0.002)。2年后,Opdivo+Yervoy组患者存活率为41%,化疗组为27%。
组织学是间皮瘤的一个公认的预后因素,非上皮样患者通常预后较差。在CheckMate-743研究中,Opdivo+Yervoy在非上皮样和上皮样MPM中均显示出总生存期的提高,在非上皮样亚组中观察到更大的生存益处。具体数据为:Opdivo+Yervoy治疗的上皮样患者的中位OS为18.7个月、非上皮样患者的中位OS为18.1个月,化疗治疗的上皮样患者中位OS为16.5个月、非上皮患者的中位OS为8.8个月(上皮样亚组:HR=0.86[95%CI:0.69,1.08];非上皮样亚组:HR=0.46[95%CI:0.31,0.68])。
该研究中,Opdivo+Yervoy双重免疫疗法的安全性与先前报告的研究一致,未观察到新的安全信号。
CheckMate-743研究结果
恶性胸膜间皮瘤(MPM)是一种罕见的、具侵袭性的肿瘤,形成于肺衬里。该病常见的发生原因与职业或生活环境中吸入石棉相关。MPM在石棉暴露后大约30-50年后发生,其诊断常常被延迟,大多数患者在就诊时已处于晚期或转移性疾病,预后通常很差:在先前未经治疗的晚期或转移性MPM患者中,中位生存期<1年,5年生存率约为10%。
MPM是一种毁灭性的疾病,在过去的15年中,治疗进展非常有限,标准护理是培美曲赛和顺铂联合治疗。Opdivo+Yervoy联合用药方案将成为这一患者群体的一种新治疗选择。来自CheckMate-743试验的阳性结果,证明了该方案一线治疗MPM的潜力,同时是在多种肿瘤类型中发现这一双重免疫治疗组合具有疗效和安全性的又一个例子。
Opdivo和Yervoy均为肿瘤免疫疗法(I-O),通过靶向免疫系统中不同的调控元件,利用人体自身的免疫系统对抗肿瘤,其中Opdivo靶向阻断PD-1/PD-L1通路,Yervoy则靶向阻断CTLA-4。
Opdivo+Yervoy是获得监管批准的一种双重免疫疗法,该疗法具有潜在的协同作用机制,针对2个不同的免疫检查点(PD-1和CTLA-4),并以互补的方式发挥作用。截至目前,Opdivo+Yervoy组合疗法已获批6种癌症的7个治疗适应症(黑色素瘤、肾细胞癌、结直肠癌、肝细胞癌、非小细胞肺癌),不同国家有所差别。
小野制药是Opdivo的初研发者,该公司于2011年与百时美施贵宝达成合作,授权百时美施贵宝Opdivo除日本、韩国、中国台湾之外的开发和商业化权利。在2014年7月,双方进一步扩大战略合作,开发和商业化多种免疫疗法(包括单药及组合疗法)用于日本、韩国、中国台湾的癌症患者。截至目前,Opdivo在日本、韩国、中国、美国和欧盟等60多个国家获得批准。
声明:本文版权归原作者所有,转载文章仅为传播更多信息,如作者信息标记有误,或侵犯您的版权,请联系我们,我们将在及时修改或删除内容,联系邮箱:marketing@360worldcare.com