科学家开发神经假体设备,终于实现帕金森病治疗0的突破
运动障碍是帕金森病(PD)的主要症状之一,约90%的PD患者在疾病晚期发展为严重的运动障碍,如步态障碍、平衡问题和冻结步态(freezing-of-gait)。其中严重的冻结步态表现为在起步、转身、狭窄处等复杂地形行走时突然的步态受阻,很容易导致患者跌倒,这不仅给患者的正常生活活动带来了困难,也很容易致患者受伤、增加住院和死亡风险。
遗憾的是,目前我们还没有有效的方法来解决PD患者终将面临的运动障碍问题。
多巴胺替代疗法和深脑电刺激(DBS)对运动障碍的治疗效果有限。有研究尝试通过电刺激脊椎的颈段或胸段来调节基底神经节和大脑皮层活动,但这种方法目前还无法形成通用疗法。
与这些以大脑为主要目标的疗法不同,今天要介绍的研究采用了另一种思路——直接靶向不受PD直接影响、行走行为的“终端”,腰骶部神经。
瑞典洛桑联邦理工学院的Grégoire Courtine和Jocelyne Bloch团队联合在《自然·医学》杂志发表论文,研究者们开发了一种神经植入假体装置,通过硬膜外刺激(EES)腰骶部背根神经,大幅度缓解PD导致的运动障碍。试验中一名有30年PD病史的患者已经使用了该装置2年,曾经无法自主行走,如今已经能够单独户外散步数公里。
该装置此前已经成功应用于恢复完全瘫痪者的行走能力,Courtine团队9月发表在《科学》的论文还找到了修复脊髓损伤的关键神经元。
论文题图
改善效果可谓非常之好
在之前的研究中已经证实,EES能够实时控制腿部运动神经元的活动,再现它们的自然激活。既然能够用于恢复下肢瘫痪者的行走能力,那么拿来改善PD患者的运动障碍,想来也是大有可能。
研究者首先在四氢吡啶(MPTP)诱导的非人灵长类PD模型中进行了实验,这能够相对较好地模拟人类PD患者的运动障碍。
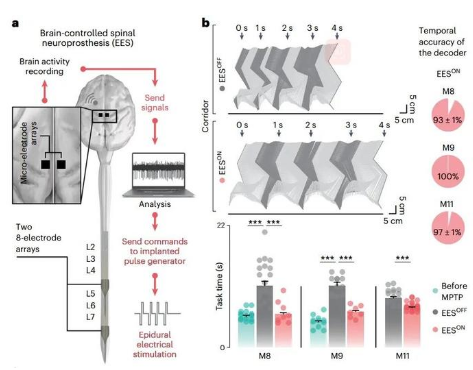
EES的作用思路,简单来说,一是要知道正常走路时腰骶部神经的作用模式,二是要能够解读身体的运动意图,以便在想要迈腿的时候激活相应的神经让腿动起来。
在动物中,前者可以记录动物健康时的神经激活模式,后者则通过监测大脑皮层活动来解码。意料之中,EES能够显著改善模式动物的步态,而且研究者们还发现,EES+DBS的组合效果甚至更好。
EES可以改善模式动物的步态问题
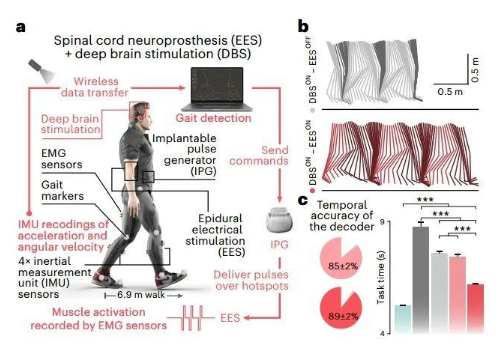
对患者来说,健康行走时的神经激活模式已经是不可能获得了,所以研究者们创建了一个神经生物动力学模型来设计神经的激活模式。由于人类受试者可以佩戴可穿戴式传感器,所以研究者们尝试通过这种非侵入性方法来解码身体的运动意图。
参与这项研究的PD患者是一位62岁的男性,他有30年PD病史,约20年前接受了DBS治疗,也使用了多巴胺替代疗法。但是这没能逆转他的疾病,到参加试验之前,他每天都会跌到5-6次,并不得不因为身体原因停止工作长时间待在家里。
令人欣喜的是,传感器已经能够达到很好的效果,患者的运动障碍大幅度改善,步态已经很接近健康人的行走模式。与动物实验一致,患者的EES+DBS联用也一定程度上提升了效果。
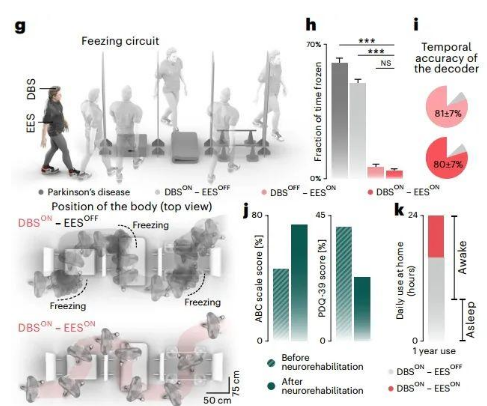
研究者们专门针对冻结步态设计了一个包括频繁转弯、躲避障碍、穿过狭窄空间的行走任务,可见在EES开启时,患者的冻结步态几乎完全消失。
过去的2年中,患者每天使用EES达到8小时,仅在长时间坐着和睡觉时关闭EES。现在,他能够在EES的帮助下,在自然中散步几公里。
患者的冻结步态问题几乎消失
考虑到DBS系统是现成的大脑植入设备,研究者们正准备尝试通过DBS来记录大脑活动,进一步优化针对冻结步态的EES刺激模式。
不过,EES仍旧是一种个性化非常强的治疗方法,是否能够应用于不同的患者还需要进一步验证。
声明:本文版权归原作者所有,转载文章仅为传播更多信息,如作者信息标记有误,或侵犯您的版权,请联系我们,我们将在及时修改或删除内容,联系邮箱:marketing@360worldcare.com