上海交大邓刘福/狄文教授团队揭示癌症免疫治疗新策略
1月31日,上海交通大学邓刘福/狄文教授研究团队在期刊《Cell Reports》上发表了题为“Cell-intrinsic PD-L1 ablation sustains effector CD8+ T cell responses and promotes antitumor T cell therapy”的研究论文,本文中,研究人员发现细胞内PD-L1信号以独立于免疫检查点功能的方式调节肿瘤进展。了解细胞内PD-L1的作用对于建立旨在克服肿瘤免疫逃避的治疗策略的基本原理是必要的。同样,阻断PD-L1核易位的药物可能潜在地增强抗pd -1治疗的抗肿瘤反应。因此,靶向细胞内PD-L1代表了一种有希望的癌症免疫治疗方法。
研究背景
免疫检查点阻断(ICB)广泛应用于肿瘤治疗。虽然一些癌症患者对ICB表现出持久应答,但原发性和获得性耐药在某些类型的癌症中常见。抗pd - l1 /抗pd -1治疗的失败归因于一系列肿瘤相关、宿主相关和肿瘤微环境因素。随着PD-L1在肿瘤微环境(TME)中的广泛表达,PD-L1与PD-1的相互作用导致了活化的CD8+ T细胞的一系列潜在命运,包括无能、耗竭和凋亡。除此之外,PD-L1/PD-1轴在调节T细胞反应中的生物学作用近期已经被确定。在典型的PD-L1/PD-1轴中,肿瘤内T细胞表面的PD-L1结合限制了巨噬细胞和其他效应T细胞的肿瘤浸润。此外,PD-L1可能具有促进T细胞生存的T细胞固有功能,这可能是由于顺式PD-L1/CD80相互作用限制了PD-1的抑制功能。考虑到PD-L1通路的多种功能,可以想象PD-L1相关机制可能有助于肿瘤免疫治疗的耐药。
细胞内PD-L1近期被发现可以独立于PD-1参与转导细胞内在信号。事实上,PD-L1的不同亚细胞定位模式可能导致各种不同的效果。另一方面,核PD-L1通过增强Gasdermin-C基因的转录将细胞凋亡转换为焦亡,导致肿瘤坏死。此外,核PD-L1影响粘附复合物的状态和基因组稳定性,导致肿瘤的侵袭性生长。显然,这些细胞内PD-L1信号以独立于免疫检查点功能的方式调节肿瘤进展。阻断PD-L1核转位的药物可能潜在地增强对抗PD-1治疗的抗肿瘤反应。因此,靶向细胞内PD-L1是一种有前途的癌症免疫治疗方法,值得进一步研究。
研究进展
越来越多的证据表明,PD-L1在T细胞介导的抗肿瘤免疫应答中发挥作用。在回顾性分析中,外周T细胞上PD-L1的表达被认为是晚期黑色素瘤患者对ICB反应性的预测性生物标志物。事实上,T细胞内的细胞内PD-L1信号传导可能导致一系列的影响。因此,靶向肿瘤浸润T细胞中的细胞内PD-L1为T细胞治疗提出了新的挑战。此外,研究人员发现治疗性T细胞过继转移后,CD103+ DCs参与了内源性CD8+ T细胞的交叉引物,这与CAR-T疗法的观察结果一致。然而,细胞内PD-L1对临床肿瘤患者肿瘤浸润CD8+ T细胞的影响尚需进一步验证。
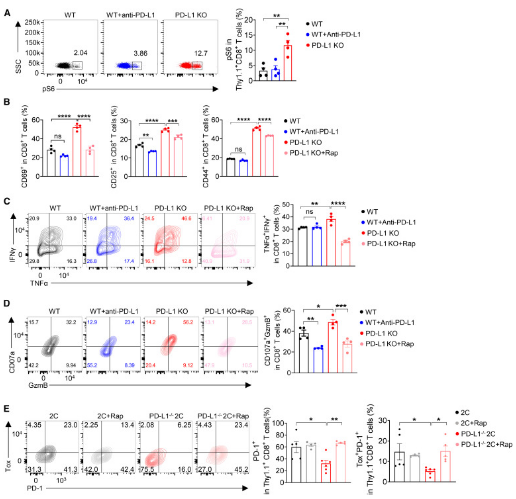
细胞内PD-L1通过mTORC1途径抑制CD8+ T细胞活性
研究结论
本研究强调了一种与PD-L1相关的机制,该机制介导了对T细胞治疗的耐药性,并为开发基于细胞内PD-L1的T细胞治疗提供了新的见解。
声明:本文版权归原作者所有,转载文章仅为传播更多信息,如作者信息标记有误,或侵犯您的版权,请联系我们,我们将在及时修改或删除内容,联系邮箱:marketing@360worldcare.com