许文荣/沈瀚团队发现胃癌进展新机制和治疗靶点
2月16日,江苏大学医学院许文荣和南京大学医学院沈瀚共同通讯在期刊《Oncogene》上在线发表题为“CircUSP1 as a novel marker promotes gastric cancer progression via stabilizing HuR to upregulate USP1 and Vimentin”的研究论文,本研究发现了一种与胃癌相关的新的环状RNA circUSP1,在胃癌组织和循环血液中表达增加,并与临床病理因素和不良预后相关。研究人员确认了circUSP1通过与致癌HuR相互作用并稳定其在转录后上调USP1和Vimentin的作用来促进胃癌的生长和转移。研究揭示了胃癌进展的新机制,并为未来胃癌诊断和治疗提供了新的潜在靶点。
研究背景
胃癌(GC)是全球第五常见的癌症,也是第四大致癌死因。幽门螺杆菌感染、饮食、外源化学物质、胃内合成的致癌物质和遗传因素被认为是胃肿瘤发生的已知风险因素,但确切机制尚未完全了解。由于早期胃癌通常没有明显症状,并且缺乏可靠的生物标志物,大多数患者在晚期被诊断,其五年生存率低于30%。此外,由于全身细胞毒性和药物耐药性,目前的治疗方法如放疗和化疗效果有限。因此,迫切需要深入了解胃癌进展的分子机制,并发现新的生物标志物和治疗靶点,以改善胃癌患者的预后。
环状RNA(circRNA)是一种具有独特环状结构的内源性RNA。它们通过前体mRNA(pre-mRNA)的反剪接过程生成,其中3'剪接受体位点连接到5'给体位点形成一个共价闭合的环状结构。近期,在各种人类组织和体液中发现了circRNA,表现出显著的稳定性、丰度、进化保守性以及组织/发育阶段特异性的表达模式。许多circRNA在多种肿瘤中失调,并参与肿瘤增殖、凋亡、迁移和侵袭。细胞质中的circRNA主要作为microRNA(miRNA)海绵,充当蛋白质翻译的模板,或与RNA结合蛋白(RBPs)相互作用,充当海绵、诱饵、支架和招募者,而核内circRNA参与基因转录调控。这些特性使circRNA具有成为有希望的生物标志物和新的癌症治疗靶点的巨大潜力。在胃癌中,越来越多的circRNA被确定为肿瘤进展的关键调节因子。因此,进一步研究与胃癌相关的circRNA将为胃癌发病机制提供宝贵的见解,并确定新的诊断和治疗策略。
研究发现
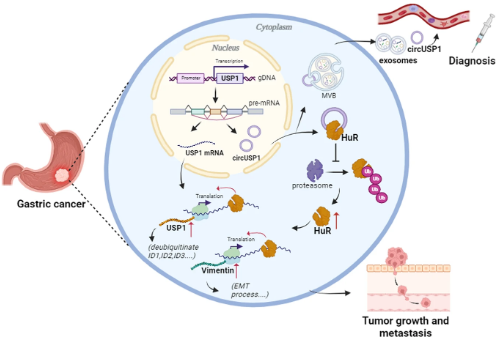
在本研究中,研究人员发现在胃癌中转录自USP1基因的一种新的环状RNA,命名为circUSP1(circBase ID: hsa_circ_000613),并探讨了其在生物学上的作用、分子机制以及在临床环境中的潜在应用。研究结果显示,circUSP1通过与稳定HuR蛋白相互作用,在转录后水平上导致USP1和Vimentin的增加,从而在促进癌症中发挥关键作用。肿瘤组织中circUSP1的增加与胃癌患者预后不良相关。研究人员发现当在血浆样本中检测到circUSP1时,它可以作为胃癌的诊断生物标志物。研究为胃癌进展机制提供了新的见解,并确定circUSP1作为胃癌的潜在生物标志物和治疗靶点。
研究结果
综上所述,本研究发现了一种与胃癌相关的新的环状RNA circUSP1,在胃癌组织和循环血液中表达增加,并与临床病理因素和不良预后相关。研究人员确认了circUSP1通过与致癌HuR相互作用并稳定其在转录后上调USP1和Vimentin的作用来促进胃癌的生长和转移。研究揭示了胃癌进展的新机制,并为未来胃癌诊断和治疗提供了新的潜在靶点。
声明:本文版权归原作者所有,转载文章仅为传播更多信息,如作者信息标记有误,或侵犯您的版权,请联系我们,我们将在及时修改或删除内容,联系邮箱:marketing@360worldcare.com