北京大学赵颖团队揭示“癌王”胰腺癌潜在治疗策略
2月27日,北京大学赵颖团队在期刊《Cell Reports》上在线发表题为“UDP-glucose dehydrogenase supports autophagy-deficient PDAC growth via increasing hyaluronic acid biosynthesis”的研究论文,在这项研究中,研究人员发现UGDH在PDAC细胞中被自噬途径降解。此外,在自噬缺陷的细胞中,积累的UGDH通过在营养匮乏状态下合成HA来支持肿瘤细胞的增殖。抑制UGDH可以减少在葡萄糖/谷氨酰胺缺乏条件下自噬缺陷细胞的生长,这可能为治疗PDAC提供了潜在前景。
研究背景
癌细胞通常生长在营养贫乏和复杂的微环境中。为了在这种营养贫乏的环境中生存和增殖,癌细胞改变代谢途径以维持其稳态。其中一种途径是自噬,这是一种进化保守的蛋白降解过程,在这个过程中,细胞内成分被包裹在自噬体内,然后被输送到溶酶体进行消化。尽管自噬提供了重要的内部营养来源,但自噬缺陷的肿瘤细胞可以通过积累自噬底物或重新连接肿瘤的代谢来存活。
例如,自噬缺陷细胞无法消除螯合体1(p62)与几种实体瘤的肿瘤发生直接相关。在谷氨酰胺缺乏情况下,自噬缺陷的肿瘤细胞利用细胞外氨基酸产生能量并存活。更重要的是,氯喹(CHQ)治疗对PDAC肿瘤生长仅有适度抑制作用。在临床试验中,自噬抑制未能改善PDAC患者的生存率。因此,自噬缺陷PDAC细胞在限制性营养条件下的生长策略需要进一步研究。
UDP-葡萄糖脱氢酶(UGDH)是一种独特的酶,能够将UDP-葡萄糖转化为UDP-葡萄糖醛酸(UDP-GlcUA),这是合成透明质酸(HA)的前体。一些研究报道UGDH上调并与癌细胞的增殖、迁移和转移有关。与正常胰腺相比,UGDH蛋白水平在小鼠和人类PDAC中显著提高。作为UGDH的下游产物,透明质酸在PDAC基质中持续升高,并在PDAC中发挥促肿瘤功能。PDAC将透明质酸代谢为N-乙酰氨基葡萄糖,以补充己糖胺生物合成途径以支持生长。此外,透明质酸结合其受体CD44或CD168,通过激活PI3K/AKT和ERK信号通路刺激肿瘤生长。
研究发现
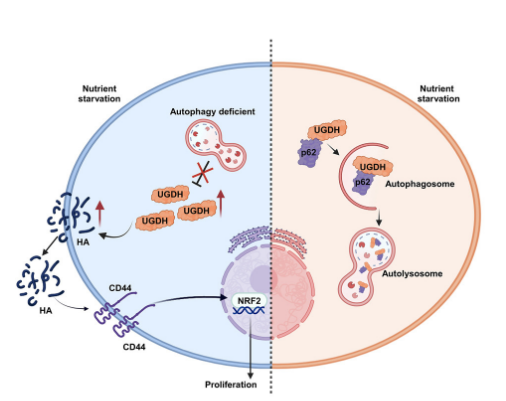
研究数据显示,在PDAC中的营养匮乏导致UDP葡萄糖脱氢酶(UGDH)降解,这依赖于自噬货物受体螯合体1(p62)。此外,研究人员证明积累的UGDH通过在能量匮乏时促进透明质酸(HA)合成,对自噬缺陷的PDAC细胞增殖至关重要。通过使用PDAC的原位小鼠模型,研究人员发现通过靶向UGDH抑制HA合成可以减轻肿瘤重量。因此,联合抑制HA和自噬可能是一种吸引人的PDAC治疗策略。
研究结论
综上所述,在这项研究中,研究人员发现UGDH在PDAC细胞中被自噬途径降解。此外,在自噬缺陷的细胞中,积累的UGDH通过在营养匮乏状态下合成HA来支持肿瘤细胞的增殖。抑制UGDH可以减少在葡萄糖/谷氨酰胺缺乏条件下自噬缺陷细胞的生长,这可能为治疗PDAC提供了潜在前景。
声明:本文版权归原作者所有,转载文章仅为传播更多信息,如作者信息标记有误,或侵犯您的版权,请联系我们,我们将在及时修改或删除内容,联系邮箱:marketing@360worldcare.com