深圳大学新研究:揭示乳腺癌靶向治疗创新策略
3月15日,深圳大学研究团队在期刊《Cell Death Discovery》上在线发表题为“Dual inhibitors of DNMT and HDAC induce viral mimicry to induce antitumour immunity in breast cancer”的研究论文,研究结果表明,15a作为一种新型有效的DNMTs和HDACs双重抑制剂具有巨大的潜力,并提高了乳腺癌体内模型的生存率。这种效应至少部分归因于病毒模拟反应的诱导。因此,15a代表了一种有前景的候选药物,用于安全有效地靶向癌症,从而为治疗各种预后不良的人类肿瘤开辟了途径。
研究背景
尽管乳腺癌的早期检测和治疗取得了显著进展,但该疾病的异质性和侵袭性使得检测和治疗具有挑战性。因此,乳腺癌仍然是女性癌症相关死亡的主要原因,仅次于肺癌。免疫检查点阻断(ICB)疗法的采用虽然在治疗黑色素瘤和肺癌方面已经取得了早期成功,但进展相对缓慢。因此,开发创新策略和治疗方法以提高患者的存活率至关重要。
在2022年发现的肿瘤特征中,非突变表观遗传重编程已经成为一种新颖特征。癌症是一种复杂的疾病,涉及遗传和表观遗传改变。表观遗传机制对癌症生物学的多个方面产生重要影响,包括促进原发肿瘤生长和侵袭,以及调节肿瘤微环境内的免疫应答。这些机制涉及DNA甲基化和组蛋白修饰之间的复杂相互作用。在参与表观遗传调控的各类酶中,DNA甲基转移酶(DNMT)和组蛋白去乙酰化酶(HDAC)尤为重要。事实上,已经开发出靶向药物,如DNMT抑制剂地西他滨和HDAC抑制剂伏立诺他(SAHA),以特异性靶向这些酶。
研究发现
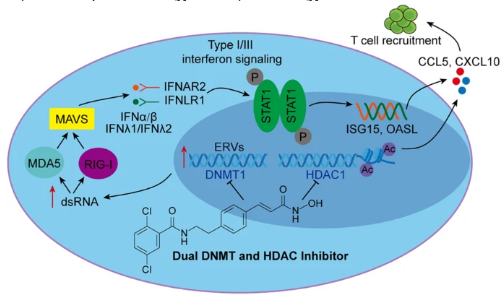
研究人员证明了DNMT 和 HDAC 在乳腺癌中过表达和正相关。DNMT和HDAC抑制剂的联合应用显示出协同的抗肿瘤效果,而研究人员先前设计的双重DNMT和HDAC抑制剂(称为DNMT/HDACi)15a在体内外能够有效抑制乳腺癌细胞的增殖、迁移和侵袭,并诱导凋亡。机制上,15a通过促进乳腺癌细胞内源逆转录病毒元件的表达诱导病毒模拟反应,从而增加细胞内双链RNA水平以激活RIG-I-MAVS通路。这进而促进干扰素和趋化因子的产生,并增强干扰素刺激基因和PD-L1的表达。15a与抗PD-L1抗体的联合在体内具有累加效应。这些发现表明,这种DNMT/HDACi具有免疫调节功能,并增强了免疫检查点阻断治疗的有效性。
研究结论
综上所述,研究结果表明,15a作为一种新型有效的DNMTs和HDACs双重抑制剂具有巨大的潜力,并提高了乳腺癌体内模型的生存率。这种效应至少部分归因于病毒模拟反应的诱导。因此,15a代表了一种有前景的候选药物,用于安全有效地靶向癌症,从而为治疗各种预后不良的人类肿瘤开辟了途径。
声明:本文版权归原作者所有,转载文章仅为传播更多信息,如作者信息标记有误,或侵犯您的版权,请联系我们,我们将在及时修改或删除内容,联系邮箱:marketing@360worldcare.com