上海交通大学等合作发现化疗耐药性乳腺癌潜在治疗方法
3月22日,上海交通大学冯海忠、李彦欣和昆明医科大学陈策实共同通讯在期刊《Molecular Cancer 》上在线发表题为“LINC00115 promotes chemoresistant breast cancer stem-like cell stemness and metastasis through SETDB1/PLK3/HIF1α signaling”的研究论文,研究结果揭示了LINC00115作为乳腺癌干细胞的关键调控因子,并强调了靶向LINC00115和SETDB1作为化疗耐药性乳腺癌的潜在治疗策略。
研究背景
癌症干细胞是癌细胞中的一个小群体,具有无限的增殖潜能和启动肿瘤克隆的能力。累积的数据表明,癌症干细胞是各种癌症(包括乳腺癌)中治疗耐药、转移和复发的关键障碍,然而其潜在机制仍然不明确。
LINC00115在包括肺腺癌、视网膜母细胞瘤、前列腺癌、卵巢癌、乳腺癌和胶质瘤在内的多种癌症中上调。LINC00115是这些癌症的预后因子。LINC00115已被确认为功能性miRNA海绵,可调控miR-200s、miR-7和miR-489-3在癌症进展中的作用。已观察到TGF-β的上调介导神经胶质瘤干细胞的干性。研究表明,LINC00115通过上调SOX9并抑制Wnt/β-catenin通路,在卵巢癌干细胞中增强干性并抑制凋亡。然而,LINC00115在治疗耐药性癌症干细胞中的作用仍未知。
HIF1α是通过促进乳腺癌干细胞表型来增强乳腺癌化疗耐药性和转移的通路的常见成分。HIF1α蛋白的稳定性和活性由一种包括蛋白激酶和蛋白/脂质磷酸酶的信号级联介导。GSK3β在氧依赖降解结构域内磷酸化HIF1α,导致HIF1α通过蛋白酶体途径增加降解。PLK3也可以通过直接与Ser576和Ser657上的HIF1α相互作用来磷酸化HIF1α,导致类似于GSK3β调控的HIF1α不稳定化。
SETDB1是一种H3K9甲基转移酶,负责组蛋白H3上的赖氨酸9甲基化,已被证明可以甲基化几种非组蛋白,如Akt。SETDB1依赖性甲基化在调节增殖、分化和细胞命运以及抑制癌症方面增强或阻碍各自的激酶活性。目前尚不清楚SETDB1在乳腺癌化疗耐药和转移中对HIF1α信号传导的重要性。
研究发现
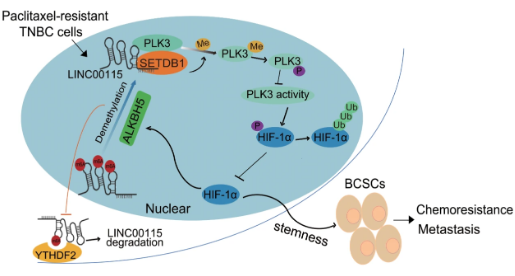
在这项研究中,研究人员对紫杉醇耐药的乳腺癌干细胞进行了全基因组lncRNA表达分析,并确定LINC00115是一个关键调节因子。结合RNA pull-down和质谱(MS)分析,研究人员展示了LINC00115作为一个支架lncRNA,通过 SETDB1/PLK3/HIF1α 信号传导调控乳腺癌干细胞的干性、化疗耐药性和转移。研究发现揭示了治疗耐药乳腺癌干细胞的一个新调控因子。
研究结论
综上所述,研究结果揭示了LINC00115作为乳腺癌干细胞的关键调控因子,并强调了靶向LINC00115和SETDB1作为化疗耐药性乳腺癌的潜在治疗策略。
声明:本文版权归原作者所有,转载文章仅为传播更多信息,如作者信息标记有误,或侵犯您的版权,请联系我们,我们将在及时修改或删除内容,联系邮箱:marketing@360worldcare.com